|
Un electrolito (o electrólito) es una sustancia que al disolverse en agua da lugar a la formación de iones. Los electrolitos pueden ser débiles o fuertes, según estén parcial o totalmente ionizados en medio acuoso.
Un electrolito fuerte es toda sustancia que al disolverse en agua se disocia completamente en iones. Por ejemplo:
| KNO3 |
→ |
NO3- |
+ |
K + |
| NaOH |
→ |
Na+ |
+ |
OH- |
| H2SO4 |
→ |
HSO4- |
+ |
H+ |
Un electrolito débil es una sustancia que al disolverse en agua se disocia parcialmente.
Por ejemplo el ácido acético:
| HAc |
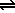 |
Ac- |
+ |
H+ |
|


