El estado interno de un sistema queda definido a partir de las magnitudes macroscópicas llamadas variables termodinámicas. Éstas puden ser la presión, la temperatura, la concentración, el volumen, la masa, la densidad...
Las variables se dividen en:
-
Intensivas. Si su valor no depende de la extensión de sistema observado. Ejemplos de tales variables son la densidad, la concentración, la presión, la temperatura...
-
Extensivas. Son las que sí dependen de la extensión de sistema considerado. Ejemplos de estas variables son la masa, el volumen, la cantdad de sustancia...
|
Por otra parte, la termodinámica se encarga únicamente de los sistemas que se encuentran en equilibrio; es decir, sistemas cuyas variables termodinámicas no varían con el tiempo y estudia el cambio sufrido por las variables del sistema entre dos estados diferentes (inicial y final).
Ecuación de estado
Hay variables de estado interdependientes. Ello permite escribir una ecuación que las relaciona y que llamamos ecuación de estado. Por ejemplo, si estudiamos un gas ideal, podemos vincular las diferentes variables de estado del siguiente modo:
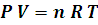
|
|
|
|


