|
A diferencia de los anteriores,
los
oxoácidos son más complejos de formular y de
nombrar. Los
oxoácidos son compuestos
ternarios,
en los que un no metal (o incluso algunos metales) se unen al
oxígeno (con valencia -2) y al hidrógeno
(con
valencia +1).
A la hora de formular el
oxoácido,
primero se escribe el hidrógeno, luego el no metal y, por
último el oxígeno. La forma correcta de
formularlos se
hace teniendo en cuenta que el oxoácido resulta de un óxido no
metálico al que se añade agua. Esto puede
ser un poco lioso, así que se puede usar la siguiente regla:
- Primero se escriben los símbolos de los
elementos: H X O (donde X es el nometal).
- Se observa la valencia del no metal:
- si es impar no se hace nada.
- si es par, se coloca un subíndice 2 al
hidrógeno.
- Se suma la valencia del no metal al número
de hidrógenos y luego se divide por 2.
- El número resultante es el
subíndice que debe llevar el oxígeno.
En la siguiente
escena podemos ver cómo se formarían, a modo de
ejemplo, los oxoácidos del cloro y del azufre:
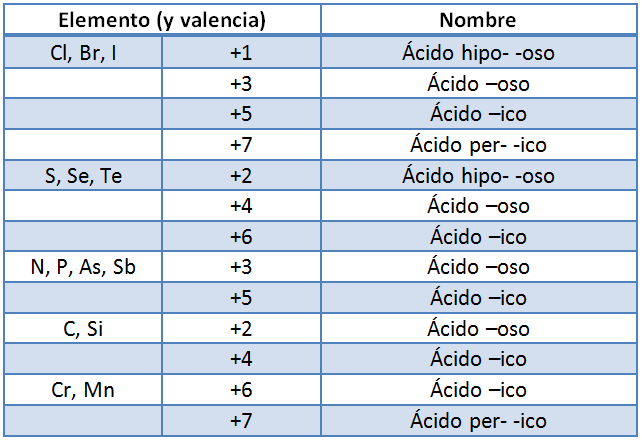
La formulación de estos compuestos es más
compleja. Veremos la forma clásica que es, a la vez, la
más común. Dependiendo de la valencia y del elemento se
usan estos prefijos y sufijos:
|