

| Formulación Inorgánica | ||
| Enrique Pescador Canora |
|
Imprimir |
| Hidruros | Objetivos |
|
El hidrógeno tiene dos valencias: +1 y -1 y puede, por tanto, formar dos tipos de compuestos. Los más abundantes son los hidruros, en los que el hidrógeno actúa con valencia negativa (-1) y de esta manera se une a todos los elementos que puedan presentar valencia positiva, a excepción del azufre, cloro, selenio, bromo, telurio y yodo. El procedimiento para formar el compuesto es el descrito en secciones anteriores, recordando que, si el subíndice de uno o de ambos elementos del compuesto debiera ser 1, no se escribe. Según el orden establecido, el símbolo del hidrógeno se debe escribir en segundo lugar (ya que es el que lleva la valencia negativa) y el símbolo del otro elemento debe escribirse en primer lugar. Para nombrar los hidruros se usa el siguiente esquema: [prefijo]hidruro de elemento Algunos hidruros se muestran en la siguiente tabla: 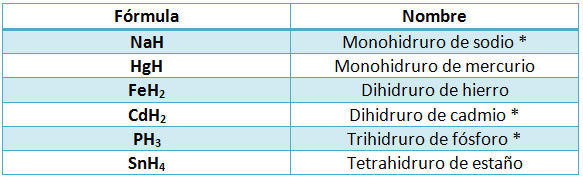 Como se
explicó en el
apartado de los óxidos, en los compuestos en los que el
elemento
que se une al hidrógeno tiene sólo una valencia,
se puede
quitar el prefijo. Es interesante ver que en HgH no se debe quitar el
prefijo para distinguirlo del dihidruro de mercurio, HgH2.
Sin embargo, para los hidruros de elementos semimetálicos y no metálicos se suelen usar nombres especiales, que son los que aparecen a continuación: 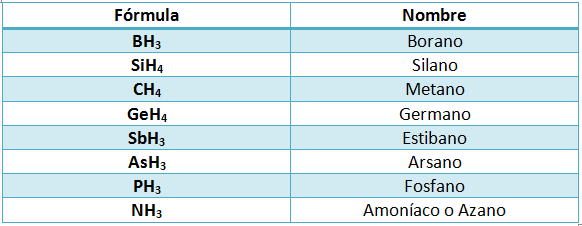
|
|