El agua pura no tiene olor, sabor, ni color, es decir, es
incolora, insípida e inodora. Su importancia reside en que
casi la totalidad de los procesos químicos que suceden en la
naturaleza, tanto en organismos vivos como en laboratorios o
en la industria tienen lugar en medio acuoso.
Henry Cavendish descubrió que el agua es una sustancia
compuesta y no un elemento como se pensaba desde la
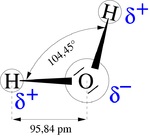
Antigüedad, Lavoisier demostró que el agua estaba formada
por oxígeno e hidrógeno y Gay Lussac junto con Von Humboldt
demostraron que el agua estaba formada por dos volúmenes de
hidrógeno y un volumen de oxígeno (H2O).
En agua se disuelven muchos compuestos, sin embargo no se
disuelven aceites y otras sustancias hidrófobas.
Las
moléculas de agua se atraen fuertemente entre si y debido a
esta interacción forman cuerpos de moléculas de agua, las
gotas.
Las moléculas de agua son capaces de mojar
(mantenerse adheridas) a otras superficies.
Las moléculas de la superficie de el agua tienen una gran
atracción creando una tensión superficial. La superficie del
líquido se comporta como una película capaz de alargarse y
al mismo tiempo ofrecer cierta resistencia al intentar
romperla. Debido a su elevada tensión superficial, algunos
insectos pueden estar sobre la superficie sin
sumergirse e, incluso, hay animales que corren, como el
basilisco.