Podemos llamar S a la solubilidad molar de una sal AnBm. Si conocemos el producto de solubilidad de la sal, podemos calcular su solubilidad. Si escribimos el equilibrio entre el precipitado y la disolución saturada del siguiente modo:
| Equilibrio |
AnBm |
|
n Am+ (ac.) + |
m Bn-(ac.) |
| Moles iniciales |
no |
|
0 |
0 |
| Moles finales |
no - (S·V) |
|
n (S·V) |
m (S·V) |
| Concentraciones finales |
|
|
n S |
m S |
Teniendo en cuenta que el producto de solubilidad se relaciona con las concentraciones de la disolución saturada:
Ks = (n S)n · (m S)m = nn· mm· S(n+m)
Por tanto la solubilidad la podemos expresar como:
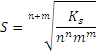
|


